использовать
Вещества с аномалиями плотности могут быть использованы в технике как компенсатор теплового расширения. При этом вещества с положительным тепловым расширением и вещества с отрицательным тепловым расширением (т.е. с аномалиями плотности) объединяются, так что при изменении температуры расширение и сжатие уравновешиваются, и материал вообще не меняет свой объем или не изменяется. точно определенным образом с температурой . Температурное расширение, близкое к нулю, гарантирует неизменную производительность при различных температурах.
Хорошим примером из повседневной жизни материалов с близким к нулю тепловым расширением является стеклокерамика — например, варочные поверхности . Б. Серан . Они обладают высокой устойчивостью к перепадам температуры , поэтому стекло не треснет, если его нагреть с одной стороны, а другая сторона находится при комнатной температуре . Это связано с тем, что некоторые фазы, содержащиеся в этой керамике, имеют аномалию плотности. Стеклокерамика регулируется с помощью химического состава таким образом, чтобы отрицательное тепловое расширение этих фаз компенсировало положительное тепловое расширение других фаз при изменении температуры. Тогда вся варочная панель практически не будет иметь теплового расширения, и Ceran не потрескается, если ее не нагреть равномерно.
Особенно в машиностроении з. Б. При производстве точных инструментов всегда ищутся материалы с максимально стабильными характеристиками в различных диапазонах температур. Особенно подходят материалы с аномалией плотности и кубической решеткой, поскольку они имеют изотропное отрицательное тепловое расширение, т.е. Это означает, что их расширение одинаково во всех трех пространственных направлениях. Примеры включают , и . В то время как в диапазоне температур от 0,3 до 1050 К имеет отрицательное тепловое расширение, проявляется в и плотность аномалии, однако, только в их фазовом начале при высокой температуре от 350 до 400 К.ZrW2О8-е{\ displaystyle {\ ce {ZrW2O8}}}ZrV2О7-е{\ displaystyle {\ ce {ZrV2O7}}}HfV2О7-е{\ displaystyle {\ ce {HfV2O7}}}ZrW2О8-е{\ displaystyle {\ ce {ZrW2O8}}}ZrV2О7-е{\ displaystyle {\ ce {ZrV2O7}}}HfV2О7-е{\ displaystyle {\ ce {HfV2O7}}}
Однако также может быть полезно проектировать материалы с точно определенным тепловым расширением
В случае дентальных имплантатов важно, чтобы пломба не расширялась в большей или меньшей степени при изменении температуры. Б
принимает горячее или холодное питье . Поэтому может быть выгодно согласовать общее расширение имплантата с расширением зубов с помощью материалов с положительным и отрицательным тепловым расширением .
Твердая фаза
Как правило, с понижением температуры вещества становятся более плотными, и вода не является исключением. Ее плотность при 25 °C составляет 0,997 г/мл и увеличивается с до максимальной (1 г/мл) при T = 4 °C. В метрической системе измерения килограмм определяется как масса 1 л воды с максимальной плотностью. Между 4 °C и точкой замерзания 0 °C происходит удивительная вещь, которая наблюдается у очень небольшого числа веществ. Вода постепенно расширяется, становясь менее плотной. Плотность льда при 0 °C составляет около 0,917 г/мл. Молекулы воды образуют кристаллы в форме тетраэдра (четырехсторонней фигуры, каждая грань которой представляет собой равносторонний треугольник). Поскольку плотность твердой фазы меньше, чем жидкой, лед плавает. При замораживании объем воды увеличивается на 1%.
Очень важно, что лед расширяется и плавает на поверхности. Из-за этого зимой лопаются водопроводы и появляются выбоины на дорогах
Замерзание и таяние воды в значительной степени ответственно за разрушение скал и образование почв. Кроме того, если бы озера и потоки замерзали снизу вверх, то водная жизнь вообще перестала бы существовать, а климатические и погодные условия резко изменились.

«Память» воды
Есть такое мнение, что вода обладает памятью, может накапливать и переносить энергию, питая тело виртуальной информацией. Длительное время данной проблемой занимался японский ученый Масару Эмото. Результаты своих исследований доктор Эмото опубликовал в книге «Послания воды». Ученым были проведены эксперименты, в рамках которых он сначала замораживал при 5 градусах каплю воды, а потом анализировал структуру кристаллов под микроскопом. Для фиксации получаемых результатов он использовал микроскоп, в который была встроена фотокамера.
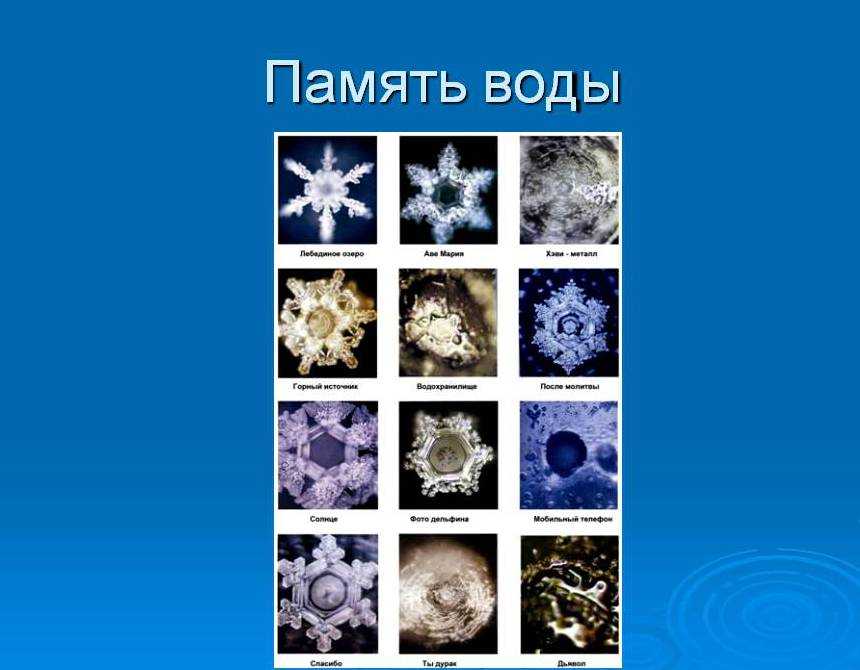
В рамках эксперимента Масау Эмото воздействовал на воду разными способами, потом заново ее замораживал, вел фотосъемку. Ему удалось получить зависимость между формой кристаллов льда и музыкой, которую “слушала” вода. Удивительно, но самые гармоничные снежинки ученый зафиксировал при использовании классической и народной музыки.
Использование современной музыки, по мнению Масау, “загрязняет” воду, поэтому им были зафиксированы кристаллы неправильной формы. Интересным фактом является и выявление японским ученым зависимости между формой кристаллов и человеческой энергией.
ПРИМЕРЫ ИСПОЛЬЗОВАНИЯ ЛЬДА
ПОЧЕМУ САМОЛЕТ ОСТАВЛЯЕТ В НЕБЕ БЕЛЫЙ СЛЕД?
В турбинах самолёта сгорает углеводородное топливо, а одним из продуктов горения является вода, ее пар, нагретый до высокой температуры. Горячие водяные пары, вылетая из сопла турбины, сразу начинают конденсироваться, образуя нитеобразное облако, состоящее из мельчайших капелек воды или кристалликов льда, т. к. температура на такой высоте ниже -40 °С. Иногда воздух на высоте бывает перенасыщен влагой, которая не может конденсироваться только из-за отсутствия так называемых ядер конденсации — мельчайших частиц, например, пыли. В таких случаях пролетающий самолёт, оставляющий за собой частицы сажи (продукт неполного сгорания топлива), вызывает конденсацию перенасыщенных паров в атмосфере. Поэтому по интенсивности белого следа от летящего самолёта можно судить о влажности воздуха в верхних слоях тропосферы, а значит, и о предстоящей погоде. Быстроисчезающий и едва заметный след говорит о том, что воздух на высоте сухой, а погода будет безоблачной. Ну а если белый след тянется через всё небо, то следует ждать ухудшения погоды. На фотографиях, сделанных со спутников, Земля во многих местах накрыта плотной белой сеткой следов от пролетевших самолётов. (См. приложение Е. ) Было показано, что в некоторых случаях следы превращаются в облака площадью от 4000 до 40 000 км2, оказывая влияние на климат. Прекращение на три дня полётов над территорией США после трагедии 11 сентября 2001 г. резко увеличило прозрачность атмосферы, в результате разница между средней дневной и ночной температурами увеличилась на градус. Таким образом, белые следы от самолётов служат одним из факторов глобального «затемнения» планеты, противодействующих её глобальному потеплению.
СНЕЖИНКИ
Привлекательность снежинок в том, что они обладают множеством мелких граней – «фасеток», на которых свет отражается и преломляется на Солнце. Каждая снежинка – монокристалл, имеющий ветвистую форму в виде шести лучей, выходящих из центрального ядра.
В данной работе мы рассмотрели свойства льда, его аномалии, загадки.
В дальнейшем планирую исследовать зависимость скорости продвижения проволоки от величины нагрузки и температуры льда. Также планирую изучить разницу поглощения энергии электромагнитного излучения (СВЧ-печи) водой и льдом. (Ответить на вопрос: «Можно ли вскипятить воду в ледяном стаканчике». )
Много удивительного установлено при изучении процессов образования и поведения льдов в природе. Как отмечал исследователь Ф. Нансен полярные льды в напряженном состоянии «кричат». Возникает легкий треск и стон, усиливаясь, они переходят через все роды тонов – лед то плачет, то стонет, то грохочет, то ревет. Постепенно возрастая, его «голос» становится подобным звучанию труб органа. Перед разрушением, при критических напряжениях лед звенит, вздыхает, ухает. Планирую установить зависимость между характером звучания льда и температурой воздуха. Это важный раздел физики льда изучен недостаточно.
Планирую изучить энергетику процессов образования и таяния льдов в природе, приблизительно оценить влияние этих процессов на изменение климата.
Лёд в природе
Изучением природных льдов во всех разновидностях на поверхности Земли, атмосфере, гидросфере, литосфере занимается наука – Гляциология.
Рассмотрим подробнее основные виды льда:
Атмосферный
Образуется в атмосфере и на земной поверхности. Выпадает на Землю в виде осадков: снега, инея, града. Также может образовать ледяные облака и туман.
Ледниковый (глетчерный)
Образуется в результате накопления и его последующего преобразования в ледяную массу. Ледники занимают 11 процентов суши. Наибольшая часть ледников расположены в Антарктиде. Самый известный шельфовый ледник Его площадь превышает 500 тыс. км2, а толщина льда достигает 700 м.
Подземный
Находится в верхней части земной коры. Основная масса находится в Северном полушарии. По подсчетам ученых запасы достигают от 0,3 до 0,5 млн км3
Морской
Образуется в море, океане при замерзании воды. Различают следующие виды:
- Припай – прикрепленный к берегу или отмели ледяной покров. Его площадь может достигать от несколько метров до тысячи километров.
- Паковый (многолетний) – морской, толщиной не менее 3 метров.
- Плавучий (дрейфующий) – это айсберги, обломки льдин.
По форме айсберги бывают столообразные и пирамидальные. Часто достигают гигантских размеров. Площадь гигантов уменьшается прогрессивно по мере их продвижения в более низкие широты.
Воде нужно больше места при ее охлаждении
В тот момент, когда начинается процесс формирования водородных связей, в воде начинают возникать места, где молекулы находятся в том же порядке, что и в кристалле льда. Эти заготовки называются кластерами. Они не прочны, как в твердом кристалле воды. При повышении температуры они разрушаются и меняют свое местоположение.
Во время процесса охлаждения воды начинает стремительно увеличиваться количество кластеров в жидкости. Они требуют больше пространства для распространения, вследствие этого вода и увеличивается в размерах после достижения своей аномальной плотности.

При падении столбика термометра ниже нуля кластеры начинают превращаться в мельчайшие кристаллы льда. Они начинают подниматься вверх. Вследствие всего этого вода превращается в лед. Это очень необычная способность воды. Данный феномен необходим для очень большого количества процессов в природе. Мы все знаем, а если не знаем, то запоминаем, что плотность льда незначительно меньше плотности прохладной или же холодной воды. Благодаря этому лед плавает на поверхности воды. Все водоемы начинают замерзать сверху вниз, что позволяет спокойно существовать и не замерзать водным обитателям на дне. Итак, теперь мы в подробностях знаем о том, расширяется или сжимается вода при замерзании.
↑йКЮЯЯХТХЙЮЖХЪ ЙЮРЮКХГЮРНПНБ
уХЛХЙХ-РЕУМНКНЦХ ОНДПЮГДЕКЪЧР ЙЮРЮКХГЮРНПШ МЮ ДБЮ РХОЮ – ЦЕРЕПНЦЕММШЕ Х ЦНЛНЦЕММШЕ. й ЦНЛНЦЕММНЛС ЙЮРЮКХГС НРМНЯЪР ОПНЖЕЯЯШ, Б ЙНРНПШУ ЙЮРЮКХГЮРНП Х ПЕЮЦХПСЧЫХЕ БЕЫЕЯРБЮ МЮУНДЪРЯЪ Б НДМНИ Х РНИ ФЕ ТЮГЕ – ФХДЙНИ ХКХ ЦЮГНБНИ – Б ЛНКЕЙСКЪПМН-ДХЯОЕПЯМНЛ ЯНЯРНЪМХХ. цЕРЕПНЦЕММШИ ЙЮРЮКХГ ПЕЮКХГСЕРЯЪ Б РЕУ ЯКСВЮЪУ, ЙНЦДЮ ЙЮРЮКХГЮРНП Х ПЕЮЦЕМРШ МЮУНДЪРЯЪ Б ПЮГМШУ ЮЦПЕЦЮРМШУ ЯНЯРНЪМХЪУ. вЮЫЕ БЯЕЦН ЙЮРЮКХГЮРНП РБ╦ПДШИ, Ю ПЕЮЦЕМРШ МЮУНДЪРЯЪ Б ЦЮГНБНИ ХКХ ФХДЙНИ ТЮГЕ. оПХМЖХОХЮКЭМЮЪ НЯНАЕММНЯРЭ ЦЕРЕПНЦЕММНЦН ЙЮРЮКХГЮ ЯНЯРНХР Б РНЛ, ВРН ПЕЮЙЖХЪ ОПНХЯУНДХР МЮ ОНБЕПУМНЯРХ РБ╦ПДНЦН ЙЮРЮКХГЮРНПЮ. бЮФМН НРЛЕРХРЭ, ВРН Б ОПНЛШЬКЕММНЯРХ ОПЕДОНВРХРЕКЭМШ ЦЕРЕПНЦЕММШЕ ЙЮРЮКХГЮРНПШ, РЮЙ ЙЮЙ НМХ ОНГБНКЪР ОПНБНДХРЭ УХЛХВЕЯЙХИ ОПНЖЕЯЯ Б МЕОПЕПШБМНЛ ПЕФХЛЕ, ОПНОСЯЙЮЪ ПЕЮЦЕМРШ ВЕПЕГ ПЕЮЙРНП, МЮОНКМЕММШИ РБ╦ПДШЛ ЙЮРЮКХГЮРНПНЛ. хЯОНКЭГНБЮМХЕ ЦНЛНЦЕММШУ ЙЮРЮКХГЮРНПНБ (НАШВМН ЩРН ПЮЯРБНПШ ЙЮРЮКХРХВЕЯЙХ ЮЙРХБМШУ ЯНЕДХМЕМХИ) БШМСФДЮЕР РЕУМНКНЦНБ ОПНБНДХРЭ УХЛХВЕЯЙХИ ОПНЖЕЯЯ Б ОЕПХНДХВЕЯЙНЛ ПЕФХЛЕ, БЙКЧВЮЧЫЕЛ ДНОНКМХРЕКЭМСЧ ЯРЮДХЧ НРДЕКЕМХЪ ОПНДСЙРНБ ПЕЮЙЖХХ НР ЙЮРЮКХГЮРНПЮ, ВРН МЕ РПЕАСЕРЯЪ Б ЯКСВЮЕ ОПХЛЕМЕМХЪ ЦЕРЕПНЦЕММШУ ЙЮРЮКХГЮРНПНБ.
уХЛХЙХ-ХЯЯКЕДНБЮРЕКХ ЙКЮЯЯХТХЖХПСЧР ЙЮРЮКХГЮРНПШ ОН ХУ УХЛХВЕЯЙНИ ОПХПНДЕ:
ЛЕРЮККШ, НЙЯХДШ, ЙХЯКНРШ Х НЯМНБЮМХЪ, ЙННПДХМЮЖХНММШЕ ЯНЕДХМЕМХЪ ОЕПЕУНДМШУ ЛЕРЮККНБ (ЛЕРЮККНЙНЛОКЕЙЯМШЕ ЙЮРЮКХГЮРНПШ), ТЕПЛЕМРШ. йХЯКНРМН-НЯМНБМШЕ, ЛЕРЮККНЙНЛОКЕЙЯМШЕ Х ТЕПЛЕМРЮРХБМШЕ ЙЮРЮКХГЮРНПШ ЛНЦСР АШРЭ ЙЮЙ ЦНЛНЦЕММШЛХ, РЮЙ Х ЦЕРЕПНЦЕММШЛХ.
бЯЕ ЙЮРЮКХГЮРНПШ УЮПЮЙРЕПХГСЧРЯЪ РПЕЛЪ ЦКЮБМШЛХ ЯБНИЯРБЮЛХ – ЮЙРХБМНЯРЭЧ, ЯЕКЕЙРХБМНЯРЭЧ Х ЯРЮАХКЭМНЯРЭЧ ДЕИЯРБХЪ.
бЯЕ РХОШ ЙЮРЮКХГЮРНПНБ ЯНДЕПФЮР РЮЙ МЮГШБЮЕЛШЕ ЮЙРХБМШЕ ЖЕМРПШ – ЮРНЛШ, ХНМШ ХКХ ЦПСООШ ЮРНЛНБ, ЙНРНПШЕ МЕОНЯПЕДЯРБЕММН БГЮХЛНДЕИЯРБСЧР Я ОПЕБПЮЫЮЧЫХЛХЯЪ ЛНКЕЙСКЮЛХ. оНМЪРХЕ НА ЮЙРХБМШУ ЖЕМРПЮУ ЙЮРЮКХГЮРНПНБ ББ╦К Б МЮСЙС ЮМЦКХИЯЙХИ СВ╦МШИ ц. рЕИКНП Б 1926 Ц. нМ СЯРЮМНБХК, ВРН РНКЭЙН 2% ОНБЕПУМНЯРХ ОКЮРХМШ НРБЕВЮЧР ГЮ ЙЮРЮКХРХВЕЯЙСЧ ЮЙРХБМНЯРЭ ЩРНЦН ЛЕРЮККЮ Б ПЕЮЙЖХЪУ НЙХЯКЕМХЪ. еЯКХ ЮЙРХБМШЕ ЖЕМРПШ АКНЙХПНБЮРЭ, ЙЮРЮКХГЮРНП РЕПЪЕР ЮЙРХБМНЯРЭ. рПЕЛЪ ЦНДЮЛХ ОНГДМЕЕ ю.ю. аЮКЮМДХМ БОЕПБШЕ ОПЕДКНФХК РЕНПХЧ ЯРПНЕМХЪ ЮЙРХБМШУ ЖЕМРПНБ ЦЕРЕПНЦЕММШУ ЙЮРЮКХГЮРНПНБ, ЙНРНПЮЪ ОНГБНКХКЮ ЕЛС ОПЕДЯЙЮГЮРЭ МЕЯЙНКЭЙН МЕХГБЕЯРМШУ ПЮМЕЕ ЙЮРЮКХГЮРНПНБ ОПНЛШЬКЕММН БЮФМШУ ОПНЖЕЯЯНБ.
б 50-Е ЦНДШ уу ЯРНКЕРХЪ ю.ю.аЮКЮМДХМ БШЯЙЮГЮК ЛШЯКЭ Н РНЛ, ВРН ЯНГДЮМХЕ РЕНПХХ ЙЮРЮКХГЮ – ЯХЯРЕЛШ МЮСВМШУ ОПЕДЯРЮБКЕМХИ, ОНГБНКЪЧЫХУ ОПЕДЯЙЮГШБЮРЭ ЮЙРХБМШЕ Х ЯЕКЕЙРХБМШЕ ЙЮРЮКХГЮРНПШ ОПНЛШЬКЕММШУ УХЛХВЕЯЙХУ ОПНЖЕЯЯНБ – ОПХБЕД╦Р Й ОЕПЕБНПНРС Б ЛЮРЕПХЮКЭМНИ ЙСКЭРСПЕ ВЕКНБЕВЕЯРБЮ. дЕИЯРБХРЕКЭМН, ПЮГПЮАНРЙЮ РЮЙНИ РЕНПХХ ОНГБНКХКЮ АШ ОПНХГБНДХРЭ МЕНАУНДХЛШЕ ДКЪ ВЕКНБЕЙЮ ЯКНФМШЕ УХЛХВЕЯЙХЕ ЯНЕДХМЕМХЪ ХГ ДЕЬ╦БНЦН Х ЬХПНЙН ПЮЯОПНЯРПЮМ╦ММНЦН ЯШПЭЪ (ОПХПНДМШИ ЦЮГ, БНДЮ, БНГДСУ, СЦКЕЙХЯКШИ ЦЮГ, ЙЮЛЕММШИ СЦНКЭ) Я ЛХМХЛЮКЭМШЛХ ГЮРПЮРЮЛХ ЩМЕПЦХХ Х Б НДМС ЯРЮДХЧ. рНЦДЮ ЯРНХЛНЯРЭ ОПНДСЙЖХХ ОПЕДОПХЪРХИ, ХЯОНКЭГСЧЫХУ УХЛХВЕЯЙХЕ ОПНЖЕЯЯШ, Ю ЩРН УХЛХВЕЯЙХЕ, МЕТРЕУХЛХВЕЯЙХЕ, ТЮПЛЮЖЕБРХВЕЯЙХЕ, ОХЫЕБШЕ ОПНХГБНДЯРБЮ, ДНКФМЮ АШКЮ АШ ПЕГЙН ОНМХГХРЭЯЪ.
й ЯНФЮКЕМХЧ, ЯНГДЮМХЕ СМХБЕПЯЮКЭМНИ НАЫЕИ РЕНПХХ ЙЮРЮКХГЮ, ЙЮЙ ЯРЮКН ЪЯМН ЕЫ╦ РПХ-ВЕРШПЕ ДЕЯЪРХКЕРХЪ РНЛС МЮГЮД, МЕБНГЛНФМН. йЮРЮКХГ – ЯКХЬЙНЛ ЯКНФМНЕ Х ЛМНЦНЮЯОЕЙРМНЕ ЪБКЕМХЕ, ЙЮРЮКХРХВЕЯЙЮЪ ЮЙРХБМНЯРЭ ГЮБХЯХР НР НВЕМЭ АНКЭЬНЦН ВХЯКЮ ТЮЙРНПНБ, БЙКЮД ЙНРНПШУ ЛЕМЪЕРЯЪ Б ГЮБХЯХЛНЯРХ НР СЯКНБХИ ОПНРЕЙЮМХЪ ОПНЖЕЯЯЮ. ьХПНЙЮЪ ПЮЯОПНЯРПЮМ╦ММНЯРЭ ЙЮРЮКХРХВЕЯЙХУ ПЕЮЙЖХИ – Ю ЛМНЦХЕ ЯОЕЖХЮКХЯРШ ОНКЮЦЮЧР, ВРН МЕЙЮРЮКХРХВЕЯЙХУ УХЛХВЕЯЙХУ ПЕЮЙЖХИ ОНОПНЯРС МЕР – ЯРЮБХР ОНД ЯНЛМЕМХЕ БНГЛНФМНЯРЭ ЯНГДЮМХЪ СМХБЕПЯЮКЭМНИ РЕНПХХ ЙЮРЮКХРХВЕЯЙНЦН ДЕИЯРБХЪ. рЕЛ МЕ ЛЕМЕЕ, ЙЮРЮКХРХВЕЯЙХЕ ПЕЮЙЖХХ АЕГСЯКНБМН ОНДВХМЪЧРЯЪ НАЫХЛ ГЮЙНМЮЛ ТХГХВЕЯЙНИ УХЛХХ.
Аномальные свойства воды и их значение для жизни
H2O является неотъемлемым компонентом существования всего живого. Это объясняет недавний интерес к обнаружению воды в других частях Вселенной. Все известные биохимические процессы происходят в водной среде. Большинство живых существ содержат 70–80% H2O по весу.
Кроме того, вода играет значительную роль в процессе фотосинтеза. Растения используют лучистую энергию солнца для превращения воды и углекислого газа в углеводы: 6CO2 + 6H2O + 672 ккал → C6H12O6 + 6O2. Фотосинтез – самая основная и важная химическая реакция на Земле. Он поставляет питательные вещества, прямо или косвенно, всем живым организмам и является основным источником атмосферного кислорода.
Аномальные свойства воды и их причины
Способность элементов формировать соединения зависит от способности их атомов отдавать или принимать электроны. Элементы первого типа становятся положительно заряженными ионами (катионами), а второго – отрицательно заряженными анионами.
Способность элемента взаимодействовать с другими элементами для образования соединений называется валентностью. Она соответствует количеству полученных или отданных электронов. Для неорганических соединений алгебраическая сумма валентных чисел элементов равна нулю. Электростатическое притяжение противоположно заряженных ионов с образованием соединения называется ионной связью.
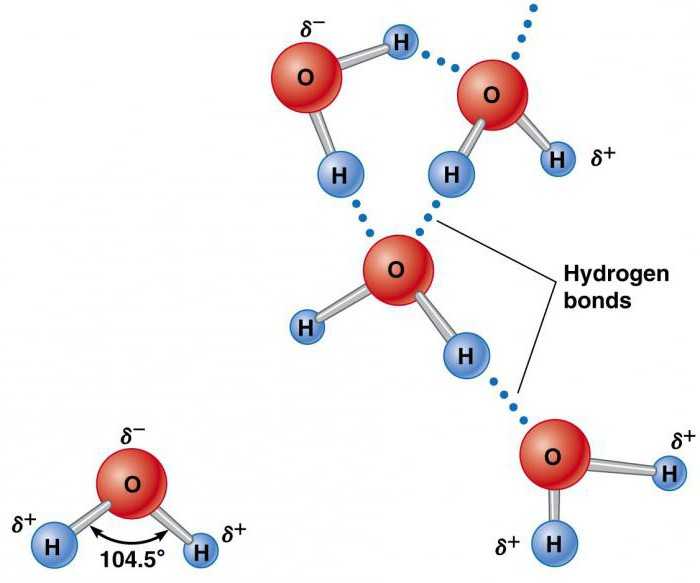
Элементы, которые образуют воду (водород и кислород), существуют отдельно в молекулах H2 и O2, содержащих по два атома. Они удерживаются вместе благодаря обмену электронной парой в химической связи, называемой ковалентной. Она намного сильнее ионной. Два атома, удерживаемые вместе ковалентной связью, образуют намного более устойчивую молекулу, чем ее составные части. В ней водород объединяется кислородом посредством общих электронных пар. Это уникальное распределение электронов в образованном химическом соединении заставляет атомы H располагаться по отношению к O под углом 104,5°.
Аномальные физические свойства воды объясняются ее структурой и химической связью.
Атом кислорода оказывает относительно сильное воздействие на общую пару электронов, в результате чего атомы водорода становятся электроположительными, а атом кислорода – электроотрицательной областью. Поскольку положительно и отрицательно заряженные участки распределены неравномерно по отношению к центральной точке, молекула воды является полярной.
Такая ее природа заставляет ее становиться электростатически привлекательной для других молекул H2O, а также ионов и контактных поверхностей с заряженными участками. Электроположительные атомы водорода притягиваются к электроотрицательным атомам кислорода соседних молекул воды. Это явление называется водородной связью. Ее прочность составляет всего около 10% ковалентной, но она отвечает за большинство аномальных физических свойств воды. К ним относятся высокие температуры замерзания и кипения, теплоемкость, удельная теплота плавления и испарения, растворимость и поверхностное натяжение.
Водородная связь отвечает за поддержание целостности молекулы H2O во время химических реакций. В то время как другие соединения подвергаются ионизации, сама вода сохраняет свою химическую целостность. Лишь относительно небольшое число молекул ионизируется в водород и гидроксильные ионы. Поэтому H2O является относительно плохим проводником электрического тока. Специфическое сопротивление теоретически чистой воды составляет 18,3 МОм∙см, в то время как питьевая имеет удельное сопротивление менее 10 000 Ом∙см. Таким образом можно легко проверить чистоту H2O.
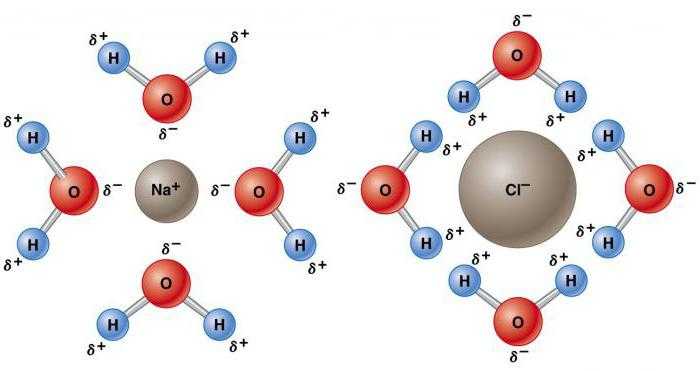
Аномальные свойства воды объясняются наличием водородных связей, из-за которых имеет место низкая плотность льда. Вдоль них при замерзании располагаются молекулы, что приводит к расширению вещества. По этой причине лед плавает на поверхности воды. Повышенное давление снижает температуру плавления. Давление, создаваемое лезвием конька, топит лед, создавая слой, обеспечивающий изящное скольжение. Даже при чрезвычайно низких температурах высокое давление ослабляет кристаллическую решетку. Это является причиной того, что огромные ледяные массы, такие как ледники, постепенно движутся.
Применение в быту
Выше упоминалось о возможности разрыва водопроводных труб при замерзании воды. Во избежание повреждения водопровода при низких температурах нельзя допускать перерывов в подаче тёплой воды, которая идёт по трубам отопления. Аналогичной опасности подвергается автотранспортное средство, если в морозы оставлять воду в радиаторе.
А теперь поговорим о приятной стороне уникальных свойств воды. Катание на коньках — большое удовольствие для детей и взрослых. А задумывались ли вы, почему лёд такой скользкий? Например, стекло тоже скользкое, к тому же глаже и привлекательнее льда. Но по нему коньки не скользят. Лишь лёд обладает таким специфическим восхитительным свойством.
Дело в том, что под тяжестью нашего веса происходит давление на тонкое лезвие конька, что, в свою очередь, вызывает давление на лёд и его таяние. При этом образуется тонкая плёнка воды, о которую и скользит стальное лезвие конька.
Различие в замерзании воска и воды
Как показывают опыты, поверхность ледяного кубика образует некую выпуклость. Это происходит из-за того, что застывание в его середине происходит в последнюю очередь. А расширяясь во время перехода в твёрдое состояние, эта выпуклость ещё больше поднимается. Противопоставить этому можно застывание воска, который, наоборот, образует углубление. Это объясняется тем, что воск после перехода в твёрдое состояние сжимается. Жидкости, которые равномерно сжимаются при промерзании, образуют несколько вогнутую поверхность.
Для замерзания воды недостаточно охладить её до точки замерзания в 0 ºС, необходимо эту температуру поддерживать за счет постоянного охлаждения.
Молекулы воды требуют больше места
Причиной тому, что происходят эти процессы расширения и сжатия различных веществ, являются молекулы. Те из них, которые получают больше энергии (это происходит в теплом помещении), двигаются намного быстрее, чем молекулы, находящиеся в холодном помещении. Частицы, которые имеют большую энергию, сталкиваются намного активнее и чаще, им необходимо больше места для движения. Чтобы сдержать то давление, которое оказывают молекулы, материал начинает увеличиваться в размерах. Причем это происходит достаточно стремительно. Итак, вода при замерзании расширяется или сжимается? Почему это происходит?
Вода не подчиняется этим правилам. Если мы начинаем охлаждать воду до четырех градусов Цельсия, то она уменьшает свой объем. Но если температура продолжает падать, то вода вдруг начинает расширяться! Существует такое свойство, как аномалия плотности воды. Это свойство возникает при температуре в четыре градуса Цельсия.

Теперь, когда мы выяснили, расширяется или сжимается вода при замерзании, давайте узнаем, как вообще возникает эта аномалия. Причина таится в частицах, из которых она состоит. Молекула воды создана из двух атомов водорода и одного — кислорода. Формулу воды все знают еще с начальных классов. Атомы в этой молекуле притягивают электроны по-разному. У водорода создается положительный центр тяжести, а у кислорода, наоборот — отрицательный. Когда молекулы воды сталкиваются друг с другом, то атомы водорода одной молекулы переходят на атом кислорода совершенно другой молекулы. Этот феномен называется водородной связью.
Значение в природе
 Тот факт, что лёд плавает на поверхности водоёмов, играет важную роль в природе. Если бы вода не обладала данным свойством и лёд погружался на дно, это привело бы к промерзанию всего водоёма и, как следствие, гибели населяющих его живых организмов.
Тот факт, что лёд плавает на поверхности водоёмов, играет важную роль в природе. Если бы вода не обладала данным свойством и лёд погружался на дно, это привело бы к промерзанию всего водоёма и, как следствие, гибели населяющих его живых организмов.
Когда наступает похолодание, сначала при температуре выше +4 ºС более холодная вода с поверхности водоёма опускается вниз, а тёплая (более лёгкая), поднимается вверх. Этот процесс называется вертикальная циркуляция (перемешивание) воды. Когда же во всём водоёме устанавливается +4 ºС, этот процесс приостанавливается, так как с поверхности вода уже при +3 ºС становится легче той, что находится ниже. Происходит расширение воды (её объём увеличивается приблизительно на 10 %) и уменьшение её плотности. Как следствие того, что более холодный слой оказывается сверху, на поверхности происходит замерзание воды и появление ледяного покрова. Вследствие своей кристаллической структуры лёд обладает плохой теплопроводностью, т. е. сдерживает тепло. Слой льда выступает своеобразным теплоизолятором. И вода, находящаяся подо льдом, сохраняет своё тепло. Благодаря теплоизоляционным свойствам льда, передача «холода» в нижние слои воды резко уменьшается
Поэтому у дна водоёма почти всегда остаётся хотя бы тонкий слой воды, что чрезвычайно важно для жизнедеятельности его обитателей
Таким образом, +4 ºС — температура максимальной плотности воды — это и есть температура выживания в водоёме живых организмов.
Основные понятия
H2O — оксид водорода, в котором содержится 11,19 % водорода, 88,81% кислорода по массе. Это бесцветная жидкость, которая не имеет ни запаха, ни вкуса. Вода является обязательным компонентом технологических процессов в промышленности.
Впервые данное вещество было синтезировано в конце 18 века Г. Кавендишем. Ученый взрывал смесь кислорода и водорода электрической дугой. Впервые проанализировал разницу в плотности льда и воды в 1612 году Г. Галилей.
В 1830 году была создана паровая машина французскими учеными П. Дюлонгом и Д. Араго. Это открытие позволило изучить взаимосвязь между давлением насыщенного пара и температурой. В 1910 году американским ученым П. Бриджменом и немцем Г. Тамманом обнаружено несколько полиморфных модификаций у льда при высоком давлении.
В 1932 году американскими учеными Г. Юри и Э. Уошберном была открыта тяжелая вода. Аномалии физических свойств данного вещества были открыты благодаря совершенствованию аппаратуры и методов проведения исследований.
Сравнение плотности воды и льда
Может ли плотность воды быть меньше плотности льда и означает ли это, что он утонет в ней? Ответ на данный вопрос утвердительный, что легко доказать следующим экспериментом.
Возьмём из морозильной камеры, где температура равна -5 ºС, кусок льда величиной в треть стакана или немного больше. Опустим его в ведро с водой температурой +20 ºС. Что мы наблюдаем? Лёд быстро погружается и тонет, постепенно начиная таять. Это происходит потому, что вода температурой +20 ºС имеет меньшую плотность по сравнению со льдом температурой -5 ºС.
Существуют модификации льда (при высоких температурах и давлениях), которые ввиду большей плотности будут в воде тонуть. Речь идёт о так называемом «тяжёлом» льде — дейтериевом и тритиевом (насыщенном тяжёлым и сверхтяжёлым водородом). Несмотря на наличие таких же пустот, как в протиевом льде, он утонет в воде. В противовес «тяжёлому» льду, протиевый лишён тяжёлых изотопов водорода и содержит 16 миллиграммов кальция на литр жидкости. Процесс его приготовления предполагает очищение от вредных примесей на 80%, благодаря чему протиевая вода считается наиболее оптимальной для жизнедеятельности человека.




























